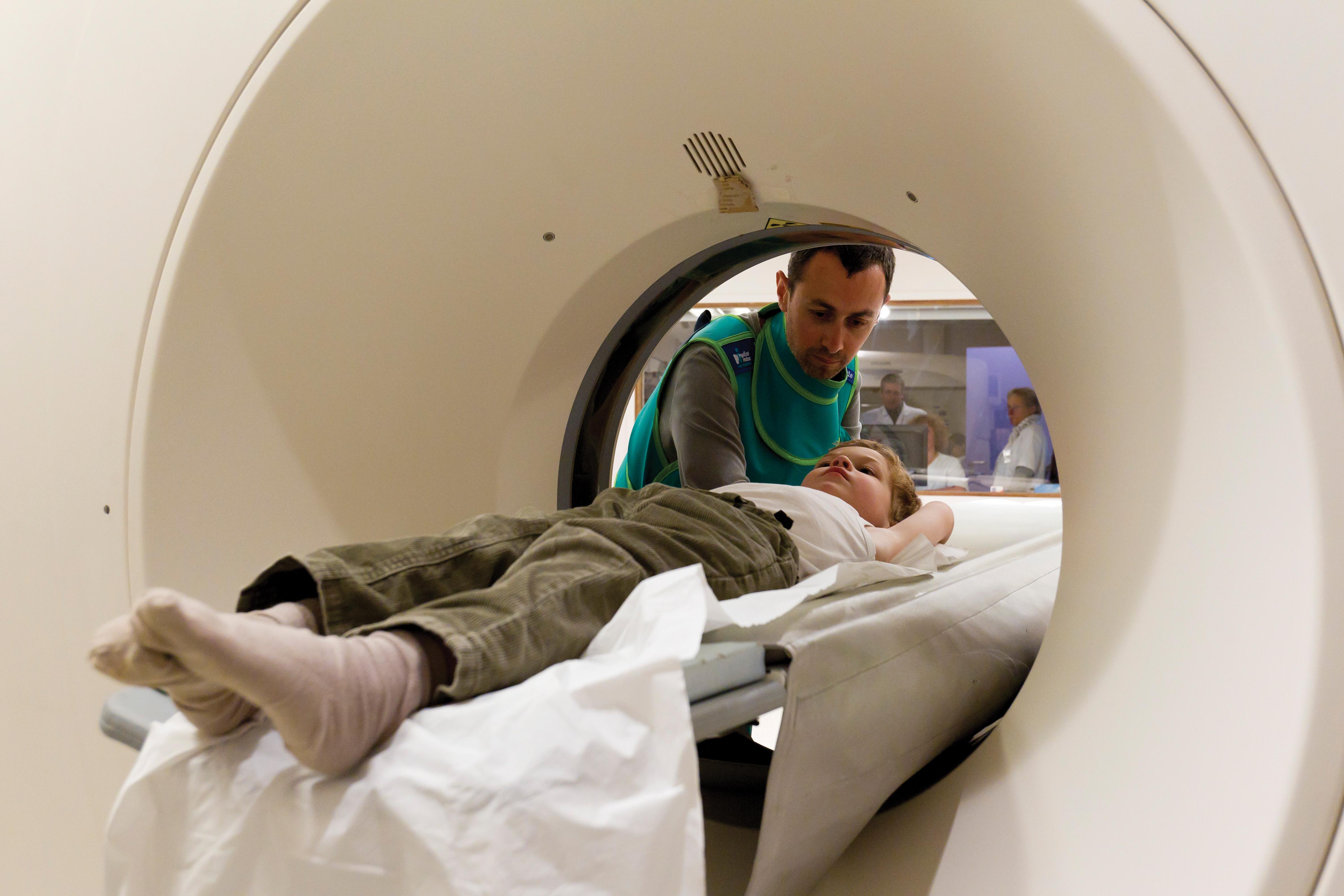
REPORTAGE - Radiothérapie innovante, mieux connaître la dose délivrée
Couplant accélérateur linéaire et IRM1, l’IRM-Linac promet des radiothérapies mieux ciblées et adaptatives. Une thèse vise à améliorer la connaissance des doses délivrées. Reportage en Côte-d’Or, à Dijon.
Avec son tunnel de 2,20 m de long, l’IRM-Linac en impose. Installé au Centre régional de lute contre le cancer Georges-François Leclerc (CGFL), à Dijon en Côte-d’Or, il réunit deux technologies. Son IRM 0,35 tesla2 aide à visualiser les tumeurs et l’accélérateur les irradie. Contrairement au guidage par scanner, « cette imagerie n’est pas ionisante », observe Louis Ermeneux, doctorant en physique médicale au Laboratoire de dosimétrie des rayonnements ionisants à Fontenay-aux-Roses (Hauts-de-Seine).
Grâce à des acquisitions IRM avant et pendant le traitement, les équipes suivent les mouvements de la tumeur. Les bénéfices attendus : une irradiation plus ciblée et un traitement délivré que lorsque la tumeur est dans l’axe du faisceau.
Mais le recul manque sur cette technologie. Le champ magnétique influence la trajectoire des particules chargées et donc la distribution de dose. Comment quantifier son impact et sa prise en compte dans le logiciel de préparation des traitements ? S’assurer qu’il n’altère pas la réponse des détecteurs mesurant les données dosimétriques ?
En 2018, le rapport IRSN 2018-00007 auquel prend part Aurélie Petitfils, physicienne médicale au CGFL, soulève ces points.
La thèse de Louis Ermeneux doit y répondre. « Nous avons besoin de dosimètres précis pour reconstituer la dose en 3D, expose-t-il, montrant un flacon au contenu pourpre. La dosimétrie par gel3 est prometteuse. » Les modifications chimiques du matériau sont proportionnelles à la dose délivrée. Son changement de couleur, lisible par scanner optique, est inadapté à la clinique. Ce protocole fonctionne pour des petits volumes. Or le volume d’un foie ou d’un pancréas est gros. L’autre moyen pour lire ces modifications chimiques est l’IRM. Pourquoi ne pas exploiter celui de la machine ? « Nous étudions la possibilité de lire ces gels et de reconstruire la dose avec l’IRM de cet appareil, moins puissant que les IRM utilisés en radiologie », indique le doctorant. Publications prévues en 2024.
1. Imagerie par résonance magnétique.
2. L’image est plus détaillée avec un champ magnétique plus fort.
3. Gel de Fricke utilise une solution ferreuse comme dosimètre.
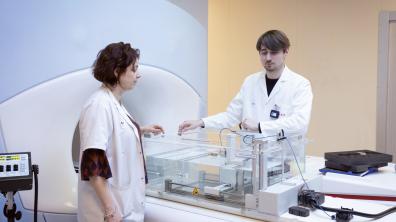
Aurélie Petitfils, physicienne médicale au Centre regional de lutte contre le cancer Georges-François Leclerc, et Louis Ermeneux, doctorant en physique médicale à l’IRSN, installent un détecteur de l’IRM-Linac. Placé dans une cuve d’eau, il mesure des doses pour caractériser le comportement du faisceau. Ce contrôle qualité est réalisé tous les mois ou deux mois. Un contrôle quotidien, plus léger, vérifie la constance de l’étalonnage de l’accélérateur.

La physicienne et le doctorant visualisent les images 3D d’IRM d’un fantôme, cube contenant du gel dosimétrique. Elles montrent les distributions de dépôt de dose, prévus par le système de planification de traitement.
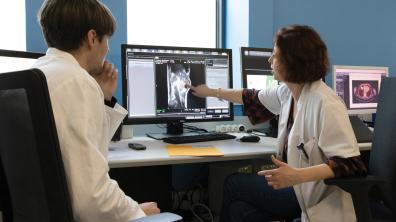
Pendant la radiothérapie, l’IRM-Linac fait des acquisitions IRM, comme celle pointée par Aurélie Petitfils. Un logiciel suit les mouvements de la tumeur. Il guide l’accélérateur linéaire afin qu’il ne délivre le faisceau de rayons X que lorsque la tumeur est en coïncidence avec ce faisceau.

Pour des tumeurs de l’abdomen, qui bougent en fonction de la respiration et du mouvement des intestins, les traitements sont adaptatifs. En fonction des mouvements de la lésion, les physiciens médicaux recalculent la dosimétrie et adaptent le plan de traitement. Zoom sur le logiciel de planification de traitement.
Photoreportage : Sophie Brädstörm/Signatures/Médiathèque IRSN
Bibliographie
Rapport N° PSE/SANTE/2018-00007
Avis 2018-00232
Avis IRSN 2021-00193
Article publié en septembre 2023